Implantes dentales
En Clínica Propdental en Barcelona, entendemos que la pérdida o el daño de los dientes puede ser una experiencia significativa para muchos. Por eso, ofrecemos servicios de implantes dentales, enfocándonos en brindar cuidados personalizados y de calidad a cada uno de nuestros pacientes.
Los implantes dentales son una solución efectiva para reemplazar dientes perdidos, proporcionando una alternativa duradera y que se integra de manera natural con tu sonrisa. En nuestra clínica, combinamos la experiencia de nuestros profesionales con tecnologías avanzadas para asegurar que cada procedimiento sea realizado con la mayor seguridad y precisión.
Nuestro equipo de especialistas está aquí para apoyarte en cada paso del camino. Desde la primera consulta, donde discutiremos tus necesidades y expectativas, hasta el seguimiento post-tratamiento, nos dedicamos a garantizar que tu experiencia sea lo más cómoda y satisfactoria posible.

¿Qué es un implante dental?
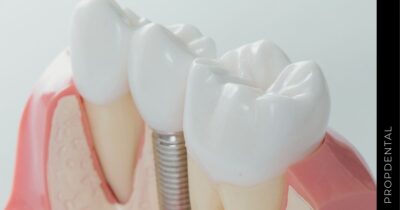
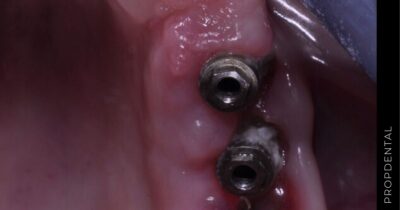
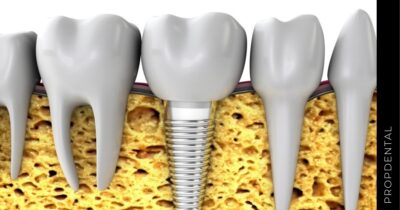
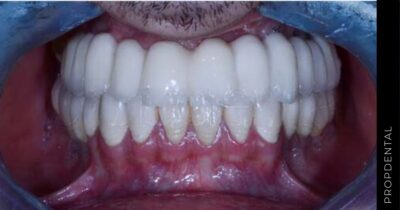
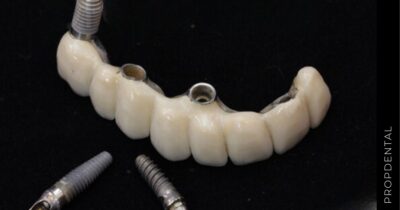
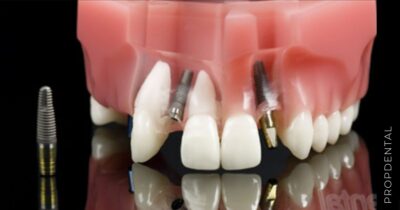
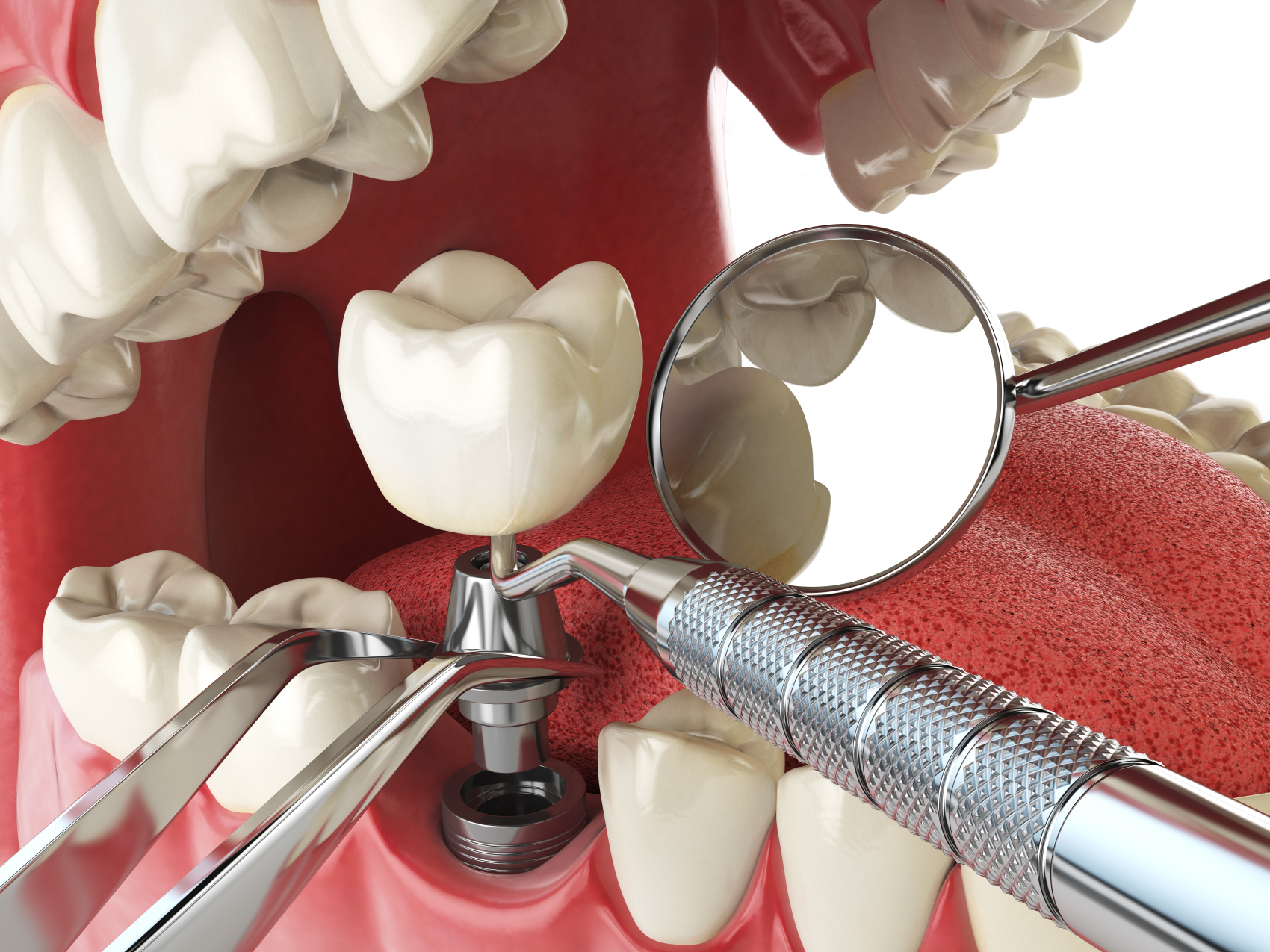
El implante dental es un producto sanitario 100% biocompatible con forma de tornillo enroscado. Este se inserta en el hueso maxilar mediante una cirugía y simula la raíz de un diente natural. Tras la fase de osteointegración (tiempo que tardará en integrarse en tu hueso alveolar), se colocará la prótesis o diente fijo definitivo. Mientras tanto, y para que no estés sin dientes en ningún momento, se hace una prótesis provisional fija (carga inmediata) o removible, que usarás mientras tanto hasta que se puedan colocar los dientes definitivos.
Por otro lado, en Clínicas Propdental ofrecemos implantes con sedación a cargo de un médico especialista, para que puedas realizar todo el tratamiento sin pasar por nervios propios, molestias o falta de confort. Trabajamos con los mejores materiales y la mayor tecnología, lo que hace que las intervenciones sean más livianas y reconfortantes.
Usamos implantes Calidad Premium NOBEL BIOCARE
Implante dental completo por 990€
¿Cómo funciona?
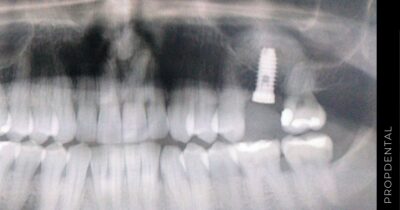
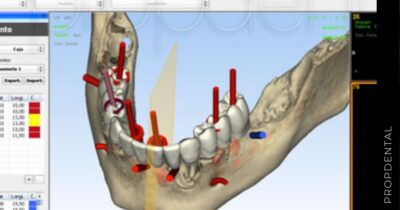
El protocolo de actuación es el siguiente: El paciente viene en una primera visita gratuita en la Clínica Propdental de Barcelona, Badalona, Hospitalet de Llobregat o Rubi. En la primera visita, hacemos una ortopantomografía y una exploración clínica para elaborar el diagnóstico y el plan de tratamiento. En esa visita, se le entrega un presupuesto del coste del tratamiento de implantología de acuerdo a sus necesidades.
Una vez aceptado el presupuesto, se le dan las citas correspondientes para la cirugía de colocación de los implantes dentales u otras cuando sean necesarias (elevación de seno o técnicas de regeneración ósea guiada). En cuanto a tratamientos de implantes con carga inmediata, se le toman las medidas el mismo día de la colocación de los implantes dentales, y al día siguiente ya puede irse con dientes fijos provisionales puestos. Una vez transcurridos de 4 a 6 meses del tiempo de osteointegración, le colocaremos las prótesis fijas definitivas.
Si quieres saber cuánto tardan en caer los puntos, visita el enlace.
PIDE CITA DESDE ESTE FORMULARIO Y OBTÉN UN DESCUENTO ESPECIAL EN TU TRATAMIENTO CON IMPLANTES POR VENIR DESDE LA WEB
Ventajas de elegir Implantes dentales
-
Aspecto natural
Logramos resultados estéticos muy naturales. -
Podrás comer con tranquilidad y naturalidad.
Ganarás en salud -
Tratamiento conservador y duradero
Es el más conservador ya que no implica dañar dientes sanos. -
Duración
Asimismo, este es el tratamiento más duradero. Si sigues los cuidados que recomendamos en Clínicas Propdental, puedes alargar la vida de tus implantes dentales para que duren muchos años. -
Natural
Es la solución fija que más se asemeja a los dientes naturales, y el porcentaje de éxito del tratamiento es del 98-95%.
El proceso de tratamiento con Implantes dentales
-
01.
Evaluación y planificación
En la primera visita gratuita en Clínicas Propdental, se realiza una evaluación completa y un diagnóstico radiológico del estado de tu boca para determinar la viabilidad de los implantes. Se planifica el tratamiento y se presenta un presupuesto acorde a tus necesidades. -
02.
Cirugía de implantes
Una vez aceptado el presupuesto, se procede a la cirugía de colocación de los implantes dentales. Esta se realiza mediante una intervención quirúrgica en la que se inserta el implante de titanio en el hueso maxilar. -
03.
Osteointegración
Después de la cirugía, el implante debe integrarse con el hueso en un proceso llamado osteointegración, que puede tardar de 4 a 6 meses. -
04.
Colocación de prótesis
Una vez que el implante ha osteointegrado adecuadamente, se procede a la colocación de las prótesis fijas definitivas. Estas prótesis son diseñadas para imitar la apariencia y función de los dientes naturales. -
05.
Seguimiento y cuidado
Después de la colocación de las prótesis, es importante seguir un adecuado cuidado oral y realizar revisiones periódicas en Clínicas Propdental para garantizar la salud y durabilidad de los implantes.
Precio de Implantes dentales
El precio de un implante dental completo es el siguiente
| Precio Implante dental completo en Propdental | Precio financiado a 60 meses sin intereses |
| 890€ | 14,83€ / mes |
Es decir: implante 490€ + corona de metal porcelana 400€ = 890€
También disponemos de coronas de circonio a un precio de 700€.
El precio de la rehabilitación completa de toda la boca (por arcada) es el siguiente
| Precio de rehabilitar toda la boca (por arcada) en Propdental | Precio financiado a 60 meses sin intereses* |
| 7740€ | 135€ / mes* |
*la financiera cobra un 5% de comisión de apertura
Es decir 6 implantes 2.940€ + coronas de metal porcelana 4.800€ = 7.740€
Si se desean coronas de circonio el precio es de 5.350€
Comparativa de precios de implantes dentales
Comparamos nuestro precios con el de algunas otras clínicas, para ello usamos como referencia el precio del implante + corona de zirconio
| Propdental | Vitaldent | Adeslas | Sanitas |
|---|---|---|---|
| 1.100 € | 1.739 € | 1.315 € | 1.587 € |
¿Por qué escoger Propdental para tu tratamiento?
-
DIAGNÓSTICO
Para saber cuánto cuesta tu tratamiento de implantes dentales es imprescindible un diagnóstico en Clínicas Propdental para valorar tu caso en particular.
-
PRIMERA VISITA GRATUITA
Hacemos tu diagnóstico y presupuesto sin coste
-
PAGOS FRACCIONADOS HASTA 60 MESES SIN INTERESES
Está sujeto a aprobación por entidad financiera.
Consejos para cuidar tus implantes
-
Evitar alimentos duros o muy calientes durante los primeros días para no poner demasiada presión en los implantes.
-
Mantener una higiene oral adecuada cepillando los dientes y las prótesis de forma suave pero meticulosa.
-
Evitar fumar y el consumo excesivo de alcohol, ya que pueden afectar negativamente la cicatrización de las heridas y la salud oral en general.
-
Asistir a las revisiones periódicas en Clínicas Propdental para asegurar el correcto mantenimiento de los implantes y la salud bucal.
Tipos de tratamiento con Implantes dentales
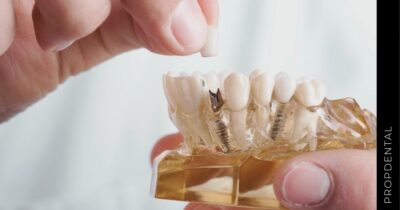
Existen distintos tipos de implantes dentales según su forma y su uso.
-
Endoóseos (o de raíz)
Actúan cómo raíces artificiales para sostener coronas (diente fijo definitivo). Están hechos de titanio o de circonio, y una vez colocados en hueso hay que esperar un periodo de 4 a 6 meses conocido como osteintegración, para que se agarre al hueso y se pueda poner el diente fijo definitivo.
-
Subperiósticos
Están indicados cuando hay una gran falta de hueso. Consiste en una estructura personalizada diseñada con un software especializado personalizados que se apoyan en la superficie de tu hueso maxilar. El nombre de implantes periósticos viene porque se coloca una estrutura de titanio personalizada y adaptada a las características de tu hueso y debajo del periostio (encía que cubre el hueso).
-
Zigomáticos
Se anclan en el hueso cigomático (pómulo). Suelen emplearse cuando hay una severa perdida de hueso maxilar. Como alternativa existen técnicas como la elevación de seno maxilar o técnicas de regeneración ósea guiada que son muy predecibles y permiten recuperar el hueso perdido.
-
De Carga Inmediata
Permiten colocar una prótesis temporal el mismo día de la cirugía. Son ideales para pacientes que quieren evitar un período sin dientes. Esta técnica es la mas empleada en Clínicas Propdental. Nos permite colocar los implantes dentales y los dientes fijos en el mismo dia.
Cada tipo de implante tiene sus propias indicaciones y requisitos, y la elección dependerá de las necesidades específicas del paciente y de la evaluación del dentista.
Preguntas frecuentes sobre Implantes dentales

- Mayor durabilidad. Mientras que la OMS (Organización Mundial de la Salud) estima que las prótesis fijas y removibles tienen una durabilidad aproximada de unos 10-15 años, los implantes pueden durar casi toda la vida.
- Mayor estabilidad y comodidad. Es como tener un diente o unos dientes propios y naturales.
- Tratamiento más conservador. Para realizar un puente o una prótesis fija, será preciso el tallado de los dientes adyacentes a la zona a rehabilitar, lo que debilitará estos dientes.
- Las prótesis removibles se sostienen mediante ganchos o ataches en las piezas dentales adyacentes a la zona a rehabilitar, lo que con el tiempo, sobrecargará estas piezas debilitándolas.
- Es el único tratamiento que permite preservar el hueso alveolar. Al perder un diente, el hueso alveolar que lo sostenía se reabsorberá o perderá con el paso del tiempo al no recibir ningún estímulo. La colocación de implantes dentales evita la reabsorción ósea en la zona edéntula (zona o área del diente perdido o ausente).
- Problemas de masticación: La ausencia de dientes puede dificultar la masticación de los alimentos, lo que afecta la digestión y la nutrición.
- Aparición de caries dental: La pérdida de un diente deja un espacio en la boca que puede ser propenso a la acumulación de restos de comida y bacterias, aumentando el riesgo de caries en los dientes vecinos.
- Pérdida de dientes colindantes: Cuando un diente se pierde, los dientes adyacentes pueden empezar a desplazarse y cambiar de posición, lo que afecta la alineación y la estética de la sonrisa.
¿Se puede poner el implante y el diente en el mismo día?
Actualmente, es posible colocar dientes fijos en un día. Esta técnica se conoce como implantes de carga inmediata. Es decir, que a las 24 horas, o el mismo momento de la colocación de los implantes de titanio, podemos colocar dientes fijos provisionales.
Los dientes de carga inmediata se colocan en el día y se llevarán durante los meses de osteointegración. Después, se colocarán los dientes fijos definitivos. Así, puedes salir de la Clínica Propdental con dientes provisionales fijos y no tienes que estar sin dientes en ningún momento. De esta forma, te puedes incorporar a tu vida social y laboral de forma inmediata. Es decir, puedes sonreír y masticar sin problemas desde el primer momento.
¿Qué alternativas existen a los implantes dentales?
Aunque los dientes permanentes deberían durar toda la vida, no todo el mundo consigue cuidar de ellos correctamente. La verdad es que hay muchos factores que pueden dañar los dientes y llevar a la pérdida de los mismos.
¿Estás acomplejado porque te falta uno o varios dientes? ¿No quieres llevar las incómodas dentaduras de quita y pon? ¿No quieres desgastar tus dientes para colocar un puente dental? Los implantes dentales son la técnica más efectiva para reemplazar los dientes perdidos. Te explicaremos todo lo que necesitas saber sobre la planificación de la mejor solución definitiva para tu caso de implantología en particular.
El implante dental mejora ampliamente las prestaciones de tu boca comparado con otros métodos más tradicionales como las dentaduras removibles de quita y pon o los puentes fijos. Las dentaduras no permiten masticar correctamente, provocan la pérdida de hueso y dañan los dientes en donde se apoyan. Los puentes tienen el inconveniente de tener que limar los dientes adyacentes en donde se apoyan.
Implantes versus puentes o dentaduras postizas
Las principales ventajas de los implantes frente a las prótesis fijas o puentes y/o a las prótesis removibles son:
¿Puedo colocarme implantes con poco hueso?
Los avances actuales también permiten colocar implantes con poco hueso. Para ello, se emplean técnicas como la elevación de seno maxilar, la regeneración ósea guiada con hueso sintético y membranas, entre otros métodos.
El tratamiento con implantes dentales en Barcelona que realizan los implantólogos de Clínicas Propdental, es una terapia altamente predecible para reponer los dientes ausentes. Incluso en los casos más complicados, como cuando tienes poco hueso, el porcentaje de éxito es muy alto.
¿Cuál es la duración de un implante dental?
Existen muchos factores que afectan a la duración de un implante dental. En primer lugar, es importante la buena colocación del implante y la calidad del hueso. Asimismo, cabe destacar la importancia que tiene la higiene y el mantenimiento que ese implante conlleva. En Clínicas Propdental consideramos que el uso de irrigador de boca es fundamental para que el paciente pueda tener una buena higiene en las prótesis sobre implantes.
El mantenimiento en el dentista debe ser como mínimo una vez al año en las Clínicas Propdental. Y por último, los malos hábitos como fumar o beber en exceso también afectan negativamente la duración del tratamiento de implantología.
¿Cuáles son los problemas de perder un diente?
Con la pérdida del diente y con el tiempo, se empieza a perder hueso en esa zona. La pérdida de un diente provoca que otros dientes se muevan y altera la capacidad para comer, dificultando así el proceso digestivo. Cuando te falta un diente, es más difícil sonreír o comer con tranquilidad, lo que puede afectar tu autoestima y confianza.
Entre los problemas más comunes que surgen debido a la pérdida de dientes se encuentran:
Licenciado en odontología. Se ha especializado con el Máster en Cirugía e implantología por la Universidad de Barcelona, y completó su formación con el Diploma de Estudios Avanzados en la Facultad de Odontología de la misma Universidad. Licenciado en Odontologia 1996-2001 Master de cirugía bucal e implantología bucofacial, Facultad de odontología, Universidad de Barcelona 2001-2004 Diploma de estudios avanzados del Doctorado con clasificación de excelente 2006.
¿Qué opinan nuestros pacientes?

Sara Hervás
Me ha encantado la clínica. Me realicé un tratamiendo dental y todo el personal fue muy amable y profesional conmigo. Repetiré sin duda!

Soffie Darken
La clínica prodental sants. Es una empresa seria, con un trato al cliente increíble y excelente trabajo. Me han puesto 2 implantes y me han quedado perfectos. Me gustó por la seriedad y la atención al cliente.

Fran C.C
Muy profesionales , buen trato y siempre muy atentos. Muy contento con mi tratamiento de implantes, sin dolor y sin problema alguno, recomendable 100%.
Testimonios de Implantes dentales
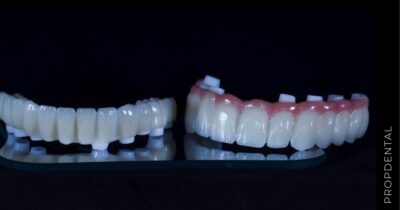
PRÓTESIS SOBRE IMPLANTES
REHABILITACIÓN CON IMPLANTES
IMPLANTES DENTALES
Tratamientos relacionados con Implantes dentales
Tratamientos destacados
Estos son los tratamientos más populares en nuestras clínicas dentales en Barcelona, Badalona, Hospitalet y Rubí